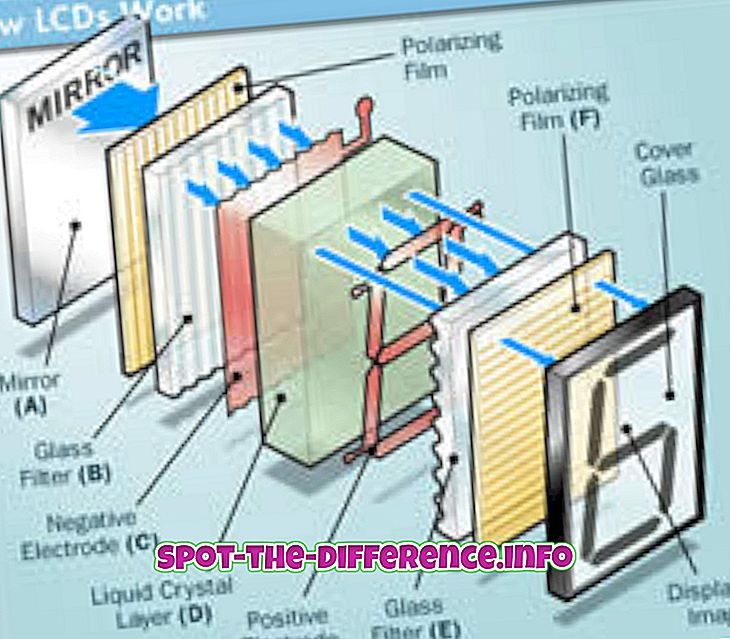
Perbedaan utama: Pedoman yang diterima secara umum adalah bahwa senyawa organik umumnya senyawa yang hampir selalu mengandung ikatan karbon-hidrogen, sedangkan segala sesuatu yang tidak diklasifikasikan sebagai senyawa anorganik. Ada beberapa pengecualian untuk aturan ini. Terutama, pembagian senyawa organik dan anorganik tergantung pada seperangkat sifat yang menentukan setiap set.

Molekul adalah jumlah terkecil dari zat kimia yang bisa ada. Seperti jumlah air terkecil yang bisa dimiliki seseorang adalah molekul air atau H20. Itu terdiri dari berbagai atom; karena itu dapat dipisahkan kembali ke atom yang berbeda.
Senyawa dibagi menjadi dua kategori utama: senyawa organik dan senyawa anorganik. Namun, masalah muncul karena selama bertahun-tahun definisi mengenai apa yang merupakan senyawa organik dan senyawa anorganik telah berbeda secara signifikan. Bahkan sekarang, tidak ada deskripsi pasti tentang apa yang cocok dalam kategori mana.
Pedoman yang diterima secara umum adalah bahwa senyawa organik umumnya senyawa yang hampir selalu mengandung ikatan karbon-hidrogen, sedangkan segala sesuatu yang tidak diklasifikasikan sebagai senyawa anorganik. Ada beberapa pengecualian untuk aturan ini. Terutama, pembagian senyawa organik dan anorganik tergantung pada seperangkat sifat yang menentukan setiap set.
Sifat umum dari Senyawa Organik dan Anorganik:
Senyawa organik | Senyawa anorganik |
Banyak gas, cairan atau padatan | Sebagian besar adalah padatan |
Biasanya selalu mengandung karbon, terutama ikatan karbon-hidrogen | Mungkin mengandung karbon. Berisi logam dan elemen lainnya. Tidak mengandung ikatan karbon-hidrogen. |
Umumnya ditemukan pada makhluk hidup, yaitu hewan dan tumbuhan. | Umumnya didapat dari benda mati, yaitu mineral. |
Secara biologis | Mineral di alam |
Beberapa senyawa sangat kompleks dan memiliki massa molekul tinggi. Senyawa kompleks ini stabil. | Senyawa anorganik kurang kompleks. Secara komparatif senyawa kompleks umumnya kurang stabil. |
Membentuk ikatan kovalen | Sebagian besar membentuk ikatan ionik, beberapa ikatan kovalen hadir |
Terdiri dari beberapa elemen saja, umumnya karbon, hidrogen, oksigen, nitrogen, belerang, dan fosfor | Terdiri dari semua elemen yang dikenal |
Tidak dapat membuat garam karena kovalen karbon | Membuat garam |
Titik leleh dan titik didih yang lebih rendah | Titik lebur dan titik didih yang lebih tinggi |
Tidak larut dalam air, larut dalam pelarut organik | Mudah larut dalam air, tidak larut dalam pelarut organik |
Sangat mudah terbakar dan tidak stabil | Tidak mudah terbakar dan tidak mudah menguap |
Konduktor panas dan listrik yang lebih buruk dalam larutan air | Konduktor panas dan listrik yang lebih baik dalam larutan air |
Laju reaksi lebih lambat | Laju reaksi lebih tinggi |
Menghasilkan rangkaian produk yang lebih kompleks selama reaksi | Menghasilkan rangkaian produk yang kurang kompleks selama reaksi |
Peragakan fenomena isomerisme | Hanya senyawa koordinasi yang menunjukkan fenomena isomerisme |
Dikelompokkan ke dalam banyak kelas berdasarkan kelompok fungsional, yang dikenal sebagai seri homolog. Setiap kelas diwakili oleh rumus umum dan anggota menunjukkan properti yang serupa. | Dikelompokkan sebagai asam, basa dan garam. Tidak ada seri homolog ditemukan |
Termasuk asam nukleat, lemak, gula, protein, enzim dan banyak bahan bakar. | Termasuk garam, logam, zat yang terbuat dari unsur tunggal dan senyawa lain yang tidak mengandung karbon yang terikat pada hidrogen. |
Contoh: metana, etana, asetilena, alkohol, karbon tetraklorida (CCl4), urea [CO (NH2) 2] | Contoh: karbon dioksida, asam sulfat, NaCl, berlian (karbon murni) |