Perbedaan utama: Susunan atom dalam molekul membantu menentukan polaritasnya. Molekul dikatakan polar, jika memiliki muatan positif dan negatif. Molekul non-polar adalah molekul dengan muatan lebih sedikit.
Dalam kimia, polaritas mengacu pada pemisahan antara muatan listrik molekul atau kelompok kimianya yang memiliki dipol listrik atau momen multi kutub. Molekul polar berinteraksi melalui ikatan intermolekul dan ikatan hidrogen. Polaritas molekul tergantung pada perbedaan elektronegativitas antara atom dalam suatu molekul. Polaritas, juga menentukan sejumlah sifat fisik seperti tegangan permukaan, titik leleh dan titik didih, dan kelarutan.
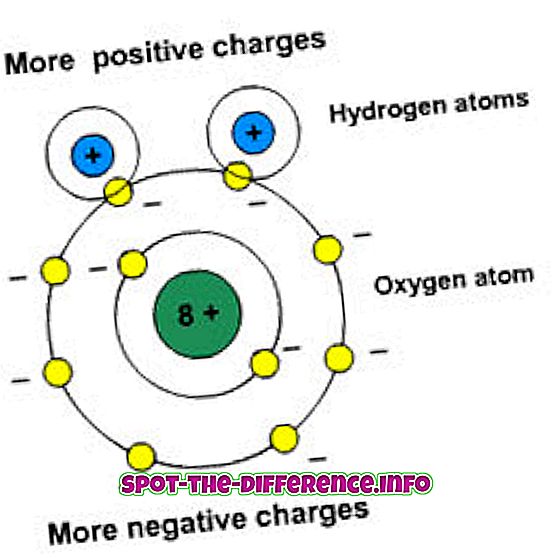
Polaritas berarti pemisahan tuntutan. Molekul-molekul ini memiliki momen dipol. Momen Dipole mengukur polaritas ikatan. Zat kutub berinteraksi dengan elemen kutub lainnya.

Molekul non-polar tidak memiliki muatan yang cukup. Molekul non-polar didistribusikan dengan cara simetri dan tidak memiliki muatan listrik yang besar. Ketika dua atom atau dua atom yang sama memiliki ikatan elektron yang sama di antara mereka, atom menarik pasangan elektron. Tarikan ini membantu mereka berbagi elektron dan jenis ikatan ikatan antara molekul dikenal sebagai ikatan kovalen non-polar.
Perbandingan antara Polar dan Non-Polar:
Kutub | Non-Polar | |
Definisi | Zat kutub memiliki muatan positif dan negatif pada atom. | Zat non-Polar tidak memiliki muatan besar pada atom yang terpasang. |
Gerakan | Mereka memiliki gerakan dipol listrik. | Mereka tidak memiliki gerakan dipol. |
Pemisahan biaya | Ada pemisahan biaya. | Tidak ada pemisahan biaya. |
Interaksi | Mereka berinteraksi dengan zat kutub lainnya. | Mereka tidak berinteraksi dengan zat kutub lainnya. |
Contoh | Air, alkohol, dan belerang. | Minyak. |