Perbedaan utama: Sel adalah sel elektrokimia yang memperoleh energi listrik dari reaksi redoks spontan di dalam sel. Baterai pada dasarnya hanyalah tumpukan atau tumpukan sel-sel elektrokimia atau galvanik.
Baterai adalah penemuan penting bagi masyarakat; mereka digunakan di hampir semua aplikasi termasuk senter, ponsel, jam, jam alarm, dll. Bayangkan sebuah dunia di mana baterai tidak ada dan semuanya akan berjalan hanya dengan listrik, jumlah kabel yang ada di sekitar akan mengganggu dan berbahaya. Baterai terus berevolusi dengan pandangan untuk mencoba menemukan zat yang dapat menahan biaya untuk waktu yang lebih lama. Baterai juga memainkan peran penting dalam mobilitas, dengan mobil listrik menjadi populer. Baterai dan sel lebih mirip, seperti sel yang memberi daya baterai, sementara baterai memberi daya pada perangkat.

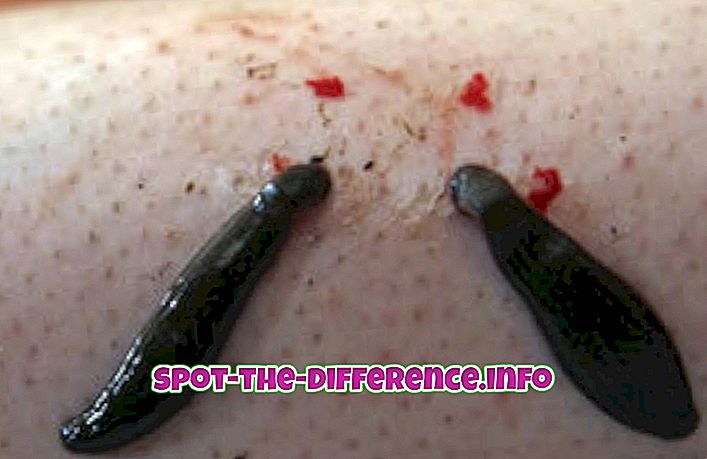
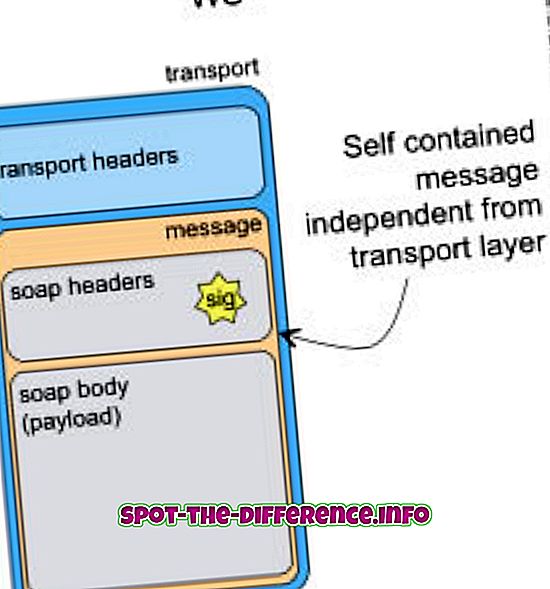
Sel elektrokimia terdiri dari dua sel setengah. Setiap setengah sel terdiri dari elektroda dan elektrolit. Kedua setengah sel itu bisa menggunakan elektrolit yang sama. Selama reaksi, spesies dari satu sel setengah kehilangan elektron (oksidasi) ke elektroda mereka sedangkan spesies setengah sel lainnya mendapatkan elektron (reduksi). Jembatan garam atau cakram berpori digunakan untuk memungkinkan kontak ion antara kedua bagian tanpa mencampur solusi. Ketika elektron ditransfer dari satu sisi ke sisi lain, perbedaan muatan ditetapkan. Jembatan garam memungkinkan ion untuk menjaga keseimbangan antara oksidasi dan reduksi. Kedua elektroda dikenal sebagai anoda dan katoda dan keduanya terhubung ke voltmeter yang resistan tinggi. Voltmeter membantu elektroda mempertahankan tegangan. Perbedaan antara muatan tersebut kemudian dikonversi menjadi energi listrik untuk digunakan dalam gadget portabel.
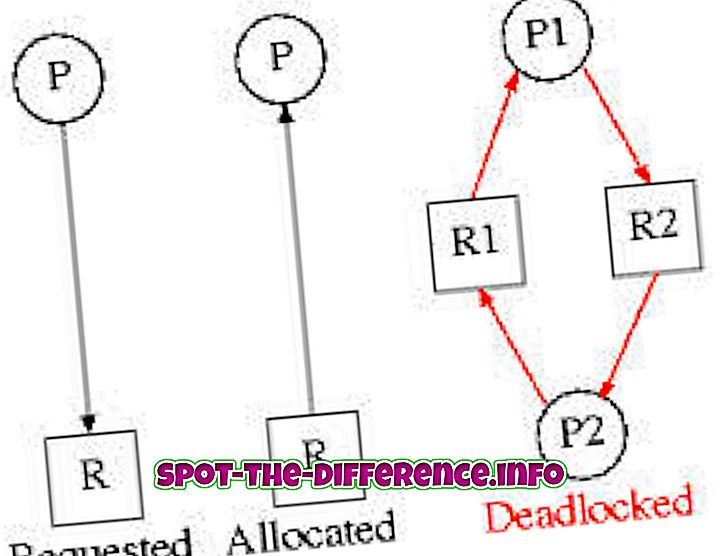
Baterai pada dasarnya hanyalah tumpukan atau tumpukan sel-sel elektrokimia atau galvanik. Fisikawan Italia Alessandro Volta dikreditkan dengan menciptakan baterai pertama pada 1800 dengan menumpuk banyak sel dalam satu seri. Istilah 'sel volta' atau 'tumpukan volta' diberikan untuk menghormati Volta. Namun, dia bukan orang yang menciptakan istilah 'baterai'. Tumpukan sel dikenal sebagai 'baterai' karena Benjamin Franklin. Dia adalah orang pertama yang menggunakan istilah 'baterai'. Franklin menggambarkan beberapa botol Leyden (yang digunakan sebagai kapasitor) sebagai baterai, merujuk analogi dengan baterai meriam. Baterai meriam biasanya merupakan istilah untuk menggambarkan garis meriam yang ditempatkan pada interval reguler untuk membuatnya mudah untuk menembak.

Ada juga berbagai jenis sel baterai yang meliputi sel basah, sel kering, garam cair dan cadangan. Baterai sel basah memiliki elektrolit cair, sedangkan sel kering memiliki elektrolit yang diimobilisasi sebagai pasta, yang hanya cukup cair untuk memungkinkan aliran elektron. Baterai garam cair menggunakan garam cair sebagai elektrolit. Ini sering digunakan dalam kendaraan listrik; namun mereka harus diisolasi dengan baik karena baterai jenis ini menghasilkan banyak panas. Baterai cadangan adalah baterai yang sering disimpan dalam bentuk yang belum dirangkai dan hanya aktif ketika bagian dalam terpasang. Baterai ini dapat disimpan untuk waktu yang lama dan seringkali merupakan bagian dari kit darurat. Baterai ini hanya menyediakan daya selama beberapa menit.
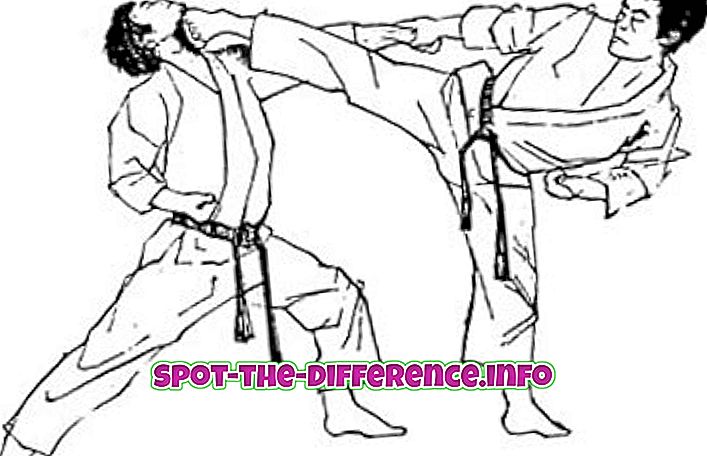
Baterai juga dapat dibuat untuk berbagai jenis bahan seperti alkali, lithium-ion, merkuri, seng-karbon, baterai nikel-seng, baterai asam timbal, sel bahan bakar, dll. Tegangan biasa untuk baterai alkaline adalah 1, 5 V dan tegangan dapat ditingkatkan dengan menambahkan lebih banyak baterai. Berbagai ukuran baterai termasuk (4.5-Volt, D, C, AA, AAA, AAAA, A23, 9-Volt, CR2032, LR44 dll.) Tergantung pada aplikasi baterai, sel-sel digabungkan untuk memberikan tegangan yang lebih tinggi, misalnya baterai 9-Volt akan memiliki 6 sel alkali dengan muatan 1, 5 V. Baterai 9-Volt digunakan pada lampu flash tugas berat. Jenis baterai yang paling umum digunakan di pasaran adalah baterai AA atau baterai AAA.